В последнее время на смену лабораторным животным и клеточным культурам в биомедицинских исследованиях приходят искусственные органы из живых клеток (микрофизиологические системы, «органы-на-чипе»). Как правило, их создание представляет собой многостадийный литографический процесс. Кроме того, в таких системах обычно нет встроенных датчиков, и наблюдать за их работой приходится с помощью внешнего оптического оборудования.
Чтобы избавить искусственный орган от этих недостатков, сотрудники Гарвардского университета прибегли к 3D-печати, разработав для этого шесть типов функциональных полимерных чернил. Все они сильно разбавлены, что позволяет печатать гибкие слои толщиной от 0,5 до 6,5 микрометра.
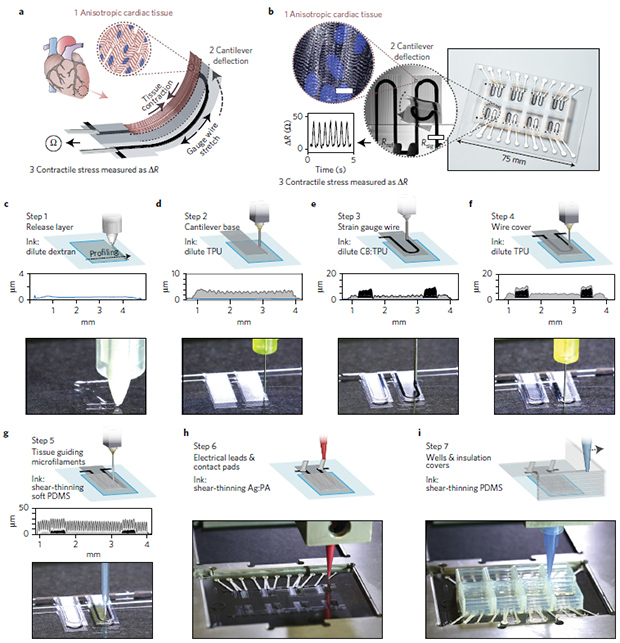
Первым слоем системы стала декстрановая пленка толщиной в 0,5 микрометра, которая служила временной растворимой подложкой для следующих слоев. Затем из термопластического полиуретана (ТПУ) ученые напечатали консоли, поддерживающие ткань. В толще этих консолей расположены эластические пьезорезистивные датчики растяжения из ТПУ с углеродными наночастицами.
На следующем этапе ученые напечатали на поверхности консолей микрофиламенты из концентрированного вязкоэластичного полидиметилсилоксана, служащие поддержкой и направляющими для роста сердечной мышечной ткани. Выступающие концы датчиков увенчали электродами с контактами из полиамида с частицами серебра. В качестве материала для изоляции электродов и восьми изолированных гибких емкостей для биологической ткани использовали полидиметилсилоксан, полилактид или акрилонитрилбутадиенстирол. Как пишут ученые, последние два материала предпочтительны для испытаний лекарств, поскольку меньше абсорбируют жирорастворимые препараты.
После этого емкости устройства заполняли миоцитами (мышечными клетками) желудочков сердца новорожденных крыс или кардиомиоцитами из человеческих индуцированных плюрипотентных стволовых клеток и помещали всю конструкцию в инкубатор с питательной средой. Благодаря филаментам с различными промежутками между ними клетки сформировали сокращающуюся ламинарную ткань, близкую по своим характеристикам реальной сердечной мышце.
В ходе экспериментов датчики успешно регистрировали интенсивность спонтанных сокращений мышечной ткани и влияние на них лекарственных препаратов (блокатора кальциевых L-каналов верапамила, уменьшающего силу и частоту сокращений, и стимулятора адреналиновых бета-рецепторов изопротеренола, увеличивающего их). Объем и зрелость мышцы из человеческих клеток стабильно повышались на протяжении 28 дней наблюдения. Система позволяет выращивать слой ткани толщиной в четыре клетки, что соответствует отдельным слоям реальной сердечной мышцы млекопитающих.
Предложенное устройство системы позволяет печатать искусственную сердечную мышцу в автоматическом режиме и без особых усилий изменять конфигурацию для конкретных задач, при этом встроенные датчики упрощают регистрацию сокращений и не требуют большого хранилища данных при долгосрочных исследованиях, как внешние оптические сенсоры, пишут ученые.
Источник: N+1